Reflexiones sobre el cribado neonatal
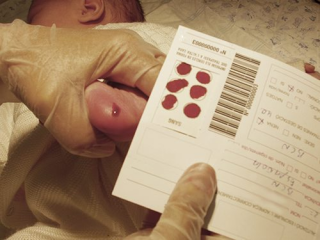
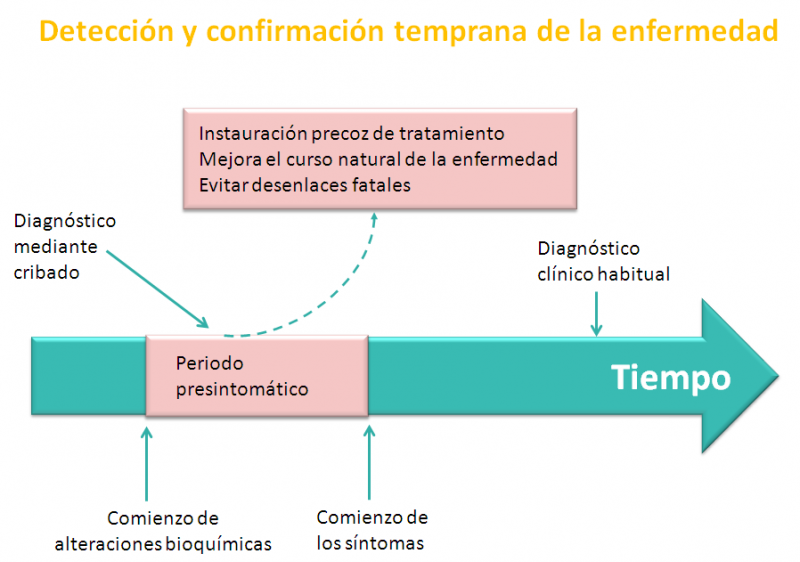
El cribado neonatal, pesquisa neonatal o screening neonatal es un conjunto de pruebas analíticas que posibilitan la detección precoz de las enfermedades, una intervención precoz para cambiar la evolución natural de las mismas y, en definitiva, mejorar la evolución de la enfermedad y la calidad de vida del paciente y sus familias.
Además, estos programas reducen el coste sanitario, ya que limitan los efectos perniciosos de la enfermedad. Esto quiere decir que son coste-efectivos.
La primera prueba que se utilizó como cribado neonatal fue descrita y desarrollada por el Dr. Robert Guthrie en 1962. Se trataba de un método sencillo para detectar fenilcetonuria en poblaciones grandes de recién nacidos (Pediatrics 1963; 32: 336-343).
Para remontarnos a los orígenes de la técnica, el Dr. Guthrie se dio cuenta de que el exceso de fenilalanina resultaba un potente inhibidor de crecimiento bacteriano. Así, cuando ponía sangre de un paciente en un cultivo de bacterias, éstas dejaban de crecer, lo que era una forma rápida de detectar el exceso de fenilalanina que se presenta en la sangre de los pacientes con fenilcetonuria.
Clásicamente existen unos criterios, llamados Criterios de Wilson-Jungner, que determinan qué características debe tener la enfermedad en la que se realice la detección y la técnica que se utilice, para ser susceptible de estar incorporado en un programa de cribado.
Estos criterios se utilizan para considerar técnicas de cribado neonatal, así como para la detección poblacional de cáncer (mamografías, test de sangre oculta en heces…, por ejemplo).
|
La enfermedad debe ser un importante problema de salud. |
|
Debe haber un tratamiento aceptado para los pacientes diagnosticados. |
|
Debe haber facilidades para el diagnóstico y tratamiento. |
|
Debe haber un periodo asintomático en la enfermedad. |
|
Debe haber una prueba disponible para su detección. |
|
La prueba debe ser aceptable para la población. |
|
Debe ser conocida la historia natural de la enfermedad. |
|
Debe haber un acuerdo sobre quién debe ser tratado como paciente |
|
El coste del diagnóstico de un caso positivo debe ser económico. |
|
La detección de un caso debe ser un proceso continuo. |
Desde que se inició la detección de los pacientes con fenilcetonuria, ha habido una evolución continua de la técnicas de detección en el recién nacido, no sólo en ECM si no también en enfermedades como el hipotiroidismo congénito, la fibrosis quística, la hiperplasia suprarrenal congénita o los déficits de audición.
En el ámbito de los ECM el verdadero cambio surgió con la incorporación de la espectrometría de masas en tándem (MS/MS) a partir de 1995. Esta técnica posibilita la detección de más de 40 enfermedades de forma simultánea gracias a la detección rápida de aminoácidos y acilcarnitinas.
Así, inicialmente se utilizaba un test para detectar un metabolito (molécula) que asociaba una enfermedad. En el momento actual un análisis permite la detección de múltiples enfermedades.
Dentro de los metabolitos que se detectan podemos hablar de primarios y secundarios, es decir, aquéllos que se alteran por efecto directo del defecto enzimático frente a los que se alteran por interferencia indirecta.
Esto hace necesaria la existencia de algoritmos de detección que contemplen los diferentes grupos de ECM, que a veces pueden compartir metabolitos alterados como marcadores directos o indirectos. Así, hay algunas similitudes entre los hallazgos analíticos de los diferentes grupos (metabolismo de los aminoácidos, defectos del ciclo de la urea, defectos de la beta oxidación o acidurias orgánicas) para los que son útiles dichos algoritmos.
Problemas para establecer la utilidad de la detección precoz
Prácticamente todos los países desarrollados han adoptado el cribado neonatal mediante MS/MS, aunque de una forma bien heterogénea. Los problemas iniciales analíticos, clínicos y de protocolo de seguimiento han sido superados, pero otros problemas de índole más ética, han surgido en la actualidad.
En este sentido queda pendiente establecer cuál es la verdadera utilidad clínica de la detección precoz en algunas enfermedades y qué enfermedades sí deben ser cribadas. A pesar de la aparente claridad de los criterios de Wilson-Jungner, la realidad es más compleja.
Las técnicas de detección precoz deben tener unos límites de detección que permitan diagnosticar a todos los pacientes aún con el riesgo de realizar algún falso positivo. Esto es, es preferible que un niño sano pase por la sospecha de estar afecto que no que un niño afecto no se diagnostique.
Estos valores hacen que la tasa de falsos negativos (niños afectos con estudio analítico normal) sea el mínimo. De esta forma, hay pacientes con alteraciones muy leves que tal vez nunca llegarían a presentar síntomas pero que sí se detectan, se les diagnostica de una enfermedad, con el estigma que esto supone y la preocupación familiar asociada. Pero en realidad se trataría de niños que tal vez tendrán una vida normal.
El cribado neonatal detecta niños que sí necesitan intervención y que si no se hace presentarán problemas de salud. Y también detecta niños que no necesitan tratamiento, sin manifestaciones clínicas evidentes. Es el caso de algunos niños que se detectan por el cribado con formas muy leves (baja penetrancia) de MCAD o con 3MCG.
En cuanto a la pregunta de qué enfermedades se deben incorporar al cribado, de nuevo la situación es complicada. Pero cada vez hay más evidencias de que enfermedades que antes no tenían tratamiento ahora, con una intervención precoz, pueden mejorar su evolución y, en presencia de una técnica adecuada, podrían ser incorporadas en el futuro.
Es el caso de la enfermedad de Wilson, la Xantomatosis cerebro tendinosa, enfermedades lisosomales, el defecto de MTHFR, la X-adrenoleucodistrofia o los defectos en el metabolismo cerebral de la creatina.
Para que los métodos analíticos sean aceptables para un programa de cribado neonatal se deben cumplir una serie de requisitos:
- Un tiempo de análisis corto, dado que el inicio temprano de las enfermedades cribadas y que se trata de pruebas universales con gran cantidad de muestra para analizar.
- Una tecnología fiable.
- Una prueba de coste no elevado.
- Ser reproducible, que se pueda llevar a cabo en otros laboratorios de la misma forma.
- Que sea sensible y específico, esto es, que identifique bien a los afectos y a los no afectos. Esto tiene que ver con los llamados falsos negativos y los falsos positivos.
Iniciativa europea para mejorar el cribado neonatal
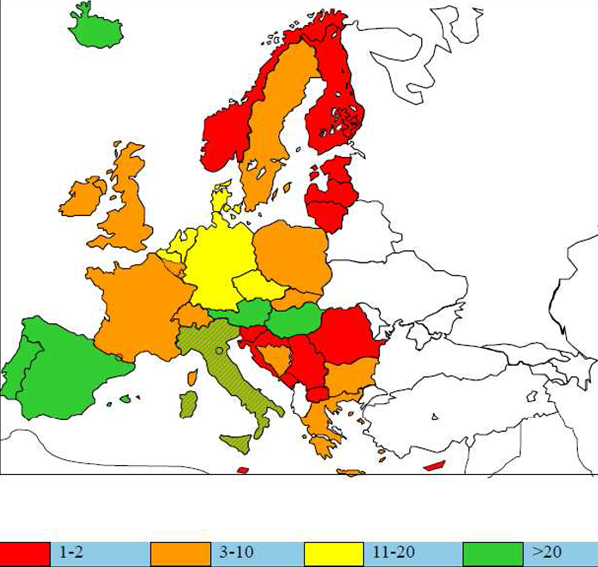
Existe un proyecto colaborativo a nivel europeo denominado MS/MS Collaborative Project en el que se comparten experiencias y conocimientos entre los laboratorios que realizan el cribado neonatal. Participan 129 laboratorios de 46 países.
Aunque cada laboratorio determina sus puntos de corte en función de su población de referencia, en ocasiones se tarda mucho tiempo en determinar estos valores, ya que se trata de enfermedades muy poco frecuentes y conseguir un número de pacientes para conocer este valor por encima del cual se debe considerar alterado, es lento.
Así, algunos de los objetivos de este proyecto colaborativo es mejorar el rendimiento analítico y alcanzar uniformidad en los metabolitos estudiados, conseguir al menos 50 muestras de cada enfermedad y evaluar y mejorar de forma continua la calidad del servicio.
La evolución del cribado neonatal ha sido rápida y favorable en los últimos años por lo que se prevé que, en el futuro, asistiremos a cambios considerables que esperamos que mejoren mucho la calidad de vida de los pacientes y sus familias.
Artículo elaborado por el Equipo de Guía Metabólica en base a las exposiciones de la Dra.Yolanda González Irazábal (Sección de Metabolopatías, Servicio de Bioquímica Clínica Hospital Miguel Servet Zaragoza) y el Dr. Hugo Rocha (Unidad Cribado Neonatal, Metabolismo y Genética, Departamento de Genética, Instituto Nacional de Saúde Doutor Ricardo Jorge, Porto, Portugal) en el VIII Simposio sobre Errores Congénitos del Metabolismo y Enfermedades Raras, Hospital Miguel Servet, Zaragoza 8 y 9 de mayo 2014.
- 2221 lecturas