Paneles génicos

Las técnicas diagnósticas están en continua evolución, sobre todo aquellas que se refieren a estudios moleculares. Cada vez más aumenta la capacidad de identificación de mutaciones en el genoma. Esto facilita mucho la confirmación de los diagnósticos de enfermedades raras. Sin embargo, aporta mucha información a veces compleja de interpretar.
Los paneles génicos, capaces de estudiar muchos genes simultáneamente, se están incorporando de forma muy rápida a la práctica clínica y ofrecen una alternativa económica y ágil frente a las técnicas más clásicas, como la secuenciación. Poco a poco se desarrollan nuevos paneles que se incorporan a las posibilidades diagnósticas de laboratorios de investigación y laboratorios de hospitales.
¿Qué es un diagnóstico genético?
El diagnostico genético es una herramienta médica que permite determinar las causas genéticas de una enfermedad.
Las enfermedades tienen unas características clínicas que la determinan como tal, diferenciándolas de otra enfermedad. Muchas enfermedades tienen base genética, es decir, la enfermedad se debe a una mutación en un gen determinado.
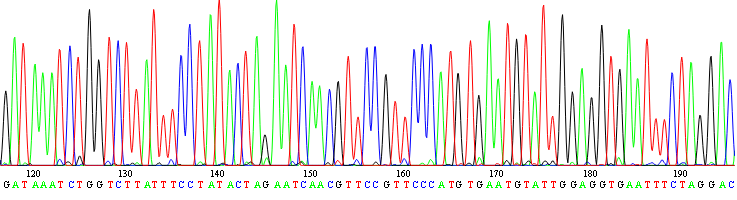
Detectar qué gen y qué mutaciones en el DNA en pacientes con enfermedades genéticas, es lo que denominamos un diagnóstico genético.
¿Qué es una mutación?
Una mutación es un cambio de pares de bases en la secuencia del DNA con respecto a la secuencia original.
Las mutaciones ocurren en todos nosotros. Todos heredamos 23 cromosomas de cada uno de nuestros padres. Estos pequeños cambios, donde uno o dos pares de bases no se alinean correctamente durante la fase temprana de la división celular ayudan a hacer que cada uno de nosotros seamos únicos.
La mayoría de los cambios genéticos se sitúan en regiones del ADN que no implican un impacto biológico, es decir, no alteran la función normal de nuestro organismo. Pero a veces la mutación se produce en un gen funcional y provoca problemas. Estos problemas son los que causan enfermedades de base genética.
Para ampliar información sobre mutaciones y DNA os recomendamos consultar los artículos Tipos de mutaciones y Del gen a la proteína.
¿Qué técnicas genéticas se utilizan?
Las técnicas genéticas están evolucionando y mejorando de manera exponencial. En los últimos 2 ó 3 años se han desarrollado técnicas de detección de mutaciones a partir de secuenciación masiva, lo que se denomina New Generation Sequencing (NGS).
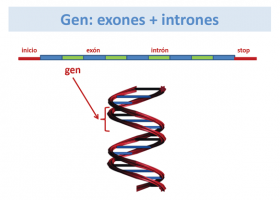
Inicialmente, esta secuenciación se realizaba en todo el DNA (high-throughput sequencing), poco tiempo después se podía realizar en sólo las regiones que contenían exones, y por tanto en la región codificante de genes (exoma) o en regiones que dan lugar a proteínas en un tejido determinado (transcriptoma, secuenciación de los transcritos).
Estas técnicas han avanzado tanto, que lo que ha quedado desplazado ha sido su interpretación, ya que se están detectando muchas variantes genéticas sin saber si hay o no repercusión fenotípica. La interpretación de los resultados encontrados es compleja y requiere de la intervención de una disciplina emergente: la bioinformática.
¿Cómo utilizar las nuevas tecnologías en la práctica clínica?
A nivel clínico, esta opción de NGS se puede usar a partir de paneles dirigidos, paneles génicos que contienen genes conocidos relacionados con la enfermedad concreta (por ejemplo, genes relacionados con las enfermedades lisosomales o con el estudio metabólico precoz neonatal).
¿Qué es un panel génico?
Un panel génico es una herramienta que nos permite detectar mutaciones en muchos genes a la vez (70 u 80 genes distintos), disminuyendo el tiempo de respuesta y el coste económico por paciente.
Hay enfermedades debidas a un único gen y otras debidas a varios genes. Por ejemplo, genes relacionados con enfermedades mitocondriales: podemos estudiar todos los genes conocidos implicados en la cadena respiratoria mitocondrial de una sola vez.
Hasta ahora, se estudiaba un gen, después otro, después otro, y así sucesivamente, hasta detectar, o no, la causa genética de una enfermedad. Esto conllevaba una gran inversión de tiempo y de dinero. Utilizando paneles génicos se disminuye el tiempo de respuesta en el diagnóstico genético, mejorando el diagnóstico precoz de enfermedades.
¿Qué ventajas tiene el panel génico frente al estudio del exoma?
En el panel génico se estudian genes elegidos, genes que ya sabemos que si están mutados pueden causar una u otra enfermedad.
El estudio del exoma nos permite saber qué mutaciones se detectan en todo el genoma, en todos los genes que tenemos, independientemente de si están relacionados con la enfermedad o no.
El estudio del exoma es sumamente interesante cuando no se conoce el gen que causa una enfermedad, ya sea porque se han estudiado todos los genes conocidos y no se ha detectado ninguna mutación o porque estemos delante de una presentación clínica nueva. Pero en la práctica rutinaria hospitalaria resulta demasiado costoso y de difícil interpretación.
Utilizando paneles génicos, ¿siempre detectamos una mutación?
No siempre. El panel génico nos permite estudiar muchos genes a la vez, y en la mayoría de los casos se detecta una mutación causante de la enfermedad que padece el paciente.
En los casos en que no se detecta ninguna mutación, es aconsejable el estudio del exoma para determinar qué gen está mutado en el paciente.
Cuando se detecta una mutación, ¿por qué debe estudiarse el resto del núcleo familiar?
Cuando se detecta una mutación en el paciente, debe estudiarse a sus padres y hermanos/as para determinar su herencia y poder ofrecer un consejo genético, así como diagnóstico prenatal en futuros embarazos. Esto es igual con el estudio de paneles génicos.
¿Por qué es importante detectar el gen y la mutación que causan la enfermedad?
Saber qué gen está mutado en cada paciente da una confirmación clínica al diagnóstico realizado por el médico.
Pero cada vez más, y se cree que en un futuro no muy lejano será así, los fármacos utilizados para tratar ciertas enfermedades van a ir relacionados con el gen mutado, el tipo de mutación en el gen, así como con la presentación clínica del paciente.
Tener un diagnóstico genético lo más precoz posible que confirme el diagnóstico clínico nos permitirá abordar la enfermedad con mucha más información, anticipando presentaciones clínicas mediante estimulación precoz o medicación preventiva, tener un seguimiento del paciente acorde con el tipo de enfermedad...
Por ejemplo, si un tipo de mutación siempre cursa con aparición de crisis epilépticas en los primeros cinco años de la enfermedad, los controles médicos pueden ser más dirigidos en detectar estas crisis, o preventivos para que no aparezcan, o seguidos en el tiempo para detectar qué tipo de crisis están apareciendo y con qué frecuencia.
Dra. Judith Armstrong. Departamento de Bioquímica y Biologia Molecular de Enfermedades Minoritarias. Hospital Sant Joan de Déu – Barcelona.
- 13801 lecturas