Opciones terapéuticas actuales (III/V) Terapia enzimática sustitutiva (09/2012)
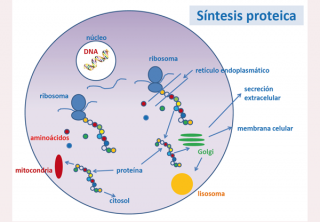
La terapia enzimática sustitutiva [del inglés: enzyme replacement therapy (ERT)] consiste en administrar periódicamente una enzima activa a un paciente con una enfermedad causada por una deficiencia enzimática con objeto de sustituir la deficitaria y corregir así el defecto.
¿Se puede aplicar esta terapia a todas las enfermedades metabólicas causadas por defectos enzimáticos?
En general las enzimas, como todas las proteínas, deben sintetizarse dentro de la célula (concretamente en el ribosoma) para que se procesen correctamente (plegarse, y modificarse por diversos procesos bioquímicos: acetilación, fosforilación, metilación, glicosilación, etc…) y puedan así dirigirse a las dianas (otras células, tejidos u orgánulos celulares), donde puedan ejercer su función enzimática de una forma eficaz.
No obstante, las enzimas lisosomales (aquéllas que actúan en el lisosoma), tanto si se producen dentro de la célula (endógenas) como fuera de ella (exógenas), tienen unas características especiales que les permiten penetrar en la célula y de allí pasar al lisosoma, su lugar de actuación.
Por esto en las enfermedades lisosomales se puede aplicar la terapia enzimática sustitutiva de forma más o menos eficaz, según la enfermedad.
¿Cuáles son las características que permiten a las enzimas lisosomales penetrar en la célula?
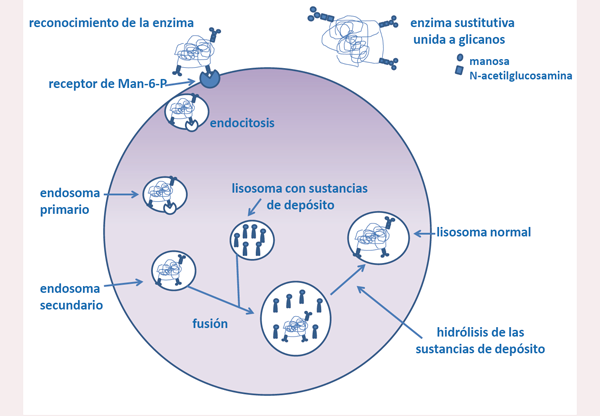
Las proteínas enzimáticas lisosomales tienen unos puntos de glicosilación (cadenas de azúcares o glicanos) que son reconocidos por unos receptores específicos de manosa-6-fosfato (Man-6-P) situados en la superficie celular.
Estas enzimas glicosiladas penetran en la célula por endocitosis (proceso de invaginación de la membrana que acaba dando lugar a un endosoma-ver dibujo) y pasan al lisosoma, donde hidrolizan (digieren o degradan) las grandes moléculas.
Cuando existe un defecto de una de las enzimas lisosomales se acumulan estas grandes moléculas dentro del lisosoma, causando enfermedades de depósito lisosomal.
Si se administran enzimas lisosomales terapéuticas debidamente glicosiladas, éstas penetran en la célula de igual forma que las enzimas endógenas originales, pasando al lisosoma y degradando en él a las sustancias de depósito acumuladas debido al defecto enzimático lisosomal que causa la enfermedad.
¿Cómo se descubrió esta característica de las enzimas lisosomales?
Se observó que cultivando células de un paciente con una mucopolisacaridosis (enfermedad lisosomal) junto con las de un individuo sano, las células del sano eran capaces de penetrar en las células del paciente y degradar las moléculas de mucopolisacárido no degradadas y acumuladas en su lisosoma, corrigiendo así el efecto de la enfermedad.
De esta observación se dedujo que se podía administrar enzimas lisosomales producidas externamente (exógenas) a un individuo enfermo para corregir su enfermedad.
¿Qué fases tiene así la terapia enzimática sustitutiva?
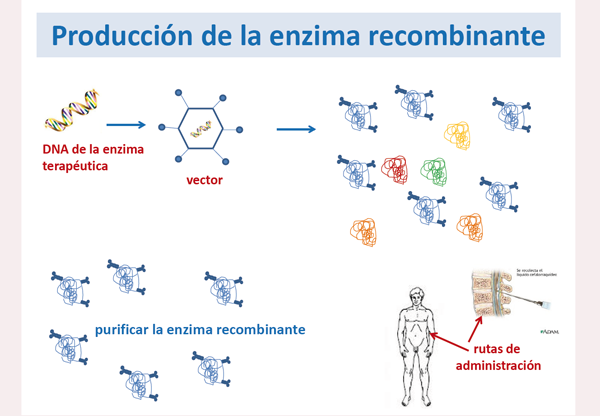
- En primer lugar se debe producir la enzima lisosomal recombinante por biotecnología, lo que representa un proceso largo y caro (ver el vídeo adjunto).
- Se debe aislar la secuencia de DNA de la enzima, es decir, separar el fragmento de DNA que contiene la información para producir una enzima correcta.
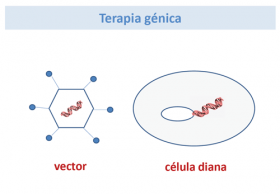
- Transferirla a un vector, es decir, introducir ese DNA con la información en un organismo (vector),
- o que pueda clonarla y reproducirla (generar muchas copias de DNA) produciendo la proteína recombinante terapéutica a gran escala (gran cantidad de proteína recombinante).
- o La proteína recombinante debe separarse del medio de cultivo y purificarse, es decir, aislarse de otras sustancias no deseadas.
- La enzima recombinante debe administrarse al paciente.
- Será reconocida por las células diana en donde actuará sustituyendo a la enzima deficiente.
- Debe corregir los efectos patogénicos del defecto enzimático, que pueden estar localizados en diversos tipos celulares del organismo del paciente (células sanguíneas, riñón, corazón, huesos, músculo, cerebro, etc…. )
¿Cómo se administra la enzima recombinante sustitutiva?
Inicialmente la administración de la enzima sustitutiva se realizaba solo por vía endovenosa, pero la demostración de que la enzima no atravesaba la barrera hematoencefálica (barrera que separa el cerebro y lo protege de sustancias y agentes nocivos), determinaba que estos tratamientos no fueran efectivos en muchas de estas enfermedades en las que el cerebro se hallaba afectado.
Por ello actualmente se administra también por vía intratecal (por punción lumbar a través del líquido cefalorraquídeo) en las enfermedades de afectación cerebral (enfermedad de Gaucher tipo II, algunas MPS).
¿En qué tipo de enfermedades se administra la terapia enzimática sustitutiva?
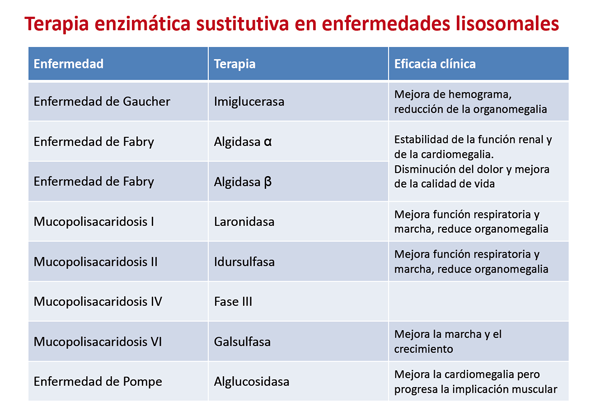
Considerando los ECM, se usa en enfermedades lisosomales, como la enfermedad de Gaucher, la de Fabry, las mucopolisacáridosis tipos I, II, IV y VI (excepto las de afectación cerebral u ósea) y la glucogenosis tipo II o enfermedad de Pompe.
No obstante, dicha terapia no es igualmente efectiva en todas ellas (Tabla 1), siendo su eficacia máxima en la enfermedad de Gaucher tipo 1, donde las células diana son macrófagos sanguíneos (un tipo de células sanguíneas con funciones de defensa).
¿Por qué no es igualmente efectiva la terapia enzimática sustitutiva en todas las enfermedades lisosomales?
Aunque todas las enfermedades lisosomales están causadas, en general, por la deficiencia de una enzima lisosomal y causan un depósito de grandes moléculas no degradadas dentro del lisosoma, clínicamente son muy heterogéneas. Pueden afectar diferentes tejidos y causar daño celular por diferentes mecanismos.
En algunas enfermedades los síntomas no solo se deben al depósito de grandes moléculas, sino también a otros efectos secundarios: inflamación, autofagia (autolesión celular por digestión), apoptosis (muerte celular programada), que no se corrigen fácilmente.
Además, la mayor parte de estas enfermedades son progresivas, de forma que el máximo efecto puede conseguirse en las primeras fases de la enfermedad.
¿Qué ventajas tiene la terapia enzimática sustitutiva sobre otros tratamientos?
Entre las ventajas se halla su fácil administración (cuando se realiza por vía endovenosa), con pocos efectos secundarios. La efectividad con bajos niveles de la enzima (1-5%) y la poca toxicidad con dosis elevadas son otras ventajas.
¿Tiene limitaciones la terapia enzimática sustitutiva?
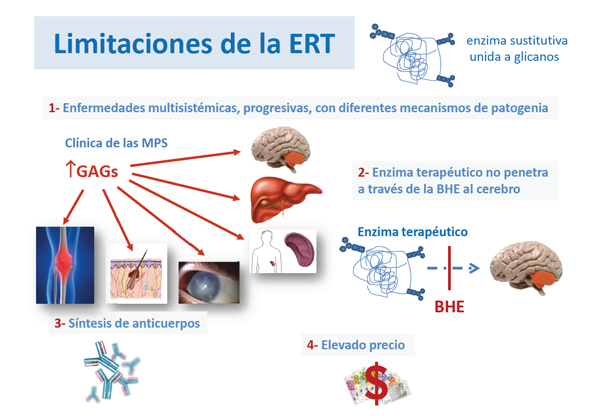
Tiene limitaciones, ya citadas, debidas a la naturaleza y progresividad de la enfermedad.
Otras limitaciones se deben al fármaco, que no puede penetrar no solo a través de la barrera hematoencefálica para alcanzar el cerebro (enfermedad de Gaucher tipo 3, algunas MPS), sino que tampoco penetra en el hueso (enfermedad de Morquio), cartílago o válvulas cardíacas, músculo (enfermedad de Pompe).
Además, al ser una proteína, provoca la síntesis de anticuerpos (sustancias que protegen al organismo contra proteínas exógenas, que pueden reducir la eficacia clínica. Por último, hay que destacar el elevado precio de dichos fármacos debido a la complejidad de su obtención y fabricación y al bajo número de pacientes que padecen estas enfermedades minoritarias.
¿Cuándo está indicado el tratamiento con terapia enzimática sustitutiva?
La indicación de iniciar un tratamiento con dicha terapia debe ser tenida en cuenta evaluando la situación clínica del paciente y su calidad de vida, las posibilidades de mejora y otras circunstancias personales.
Este hecho genera con frecuencia, en las reuniones científicas, debates éticos en los que se concluye, casi siempre, que es difícil establecer generalidades.
¿Qué estrategias se están desarrollando para mejorar la eficacia de la terapia enzimática sustitutiva?
Entre los factores esenciales para que dicha terapia sea efectiva es que la enzima terapéutica sea reconocida y captada por la célula diana, para que pueda allí ejercer su función.
Para mejorar dicho reconocimiento la célula debe expresar los receptores de Man-6-P y la enzima terapéutica debe estar correctamente glicosilada.
Dras. Mercedes Serrano y Mª. Antònia Vilaseca. Equipo Guía metabólica. Hospital Sant Joan de Déu.
- 20426 lecturas