Estrés oxidativo en las enfermedades metabólicas hereditarias (ECM)
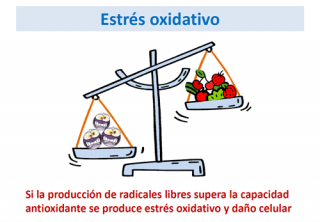
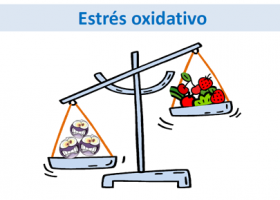
El oxígeno es indispensable para la vida de muchos organismos, entre ellos el ser humano. No obstante, si su presión es excesiva puede llegar a ser tóxico, ya que tiende a producir radicales libres. Los seres vivos han desarrollado mecanismos para protegerse del efecto tóxico del oxígeno, pero si la producción de radicales libres es muy grande y los mecanismos de defensa son insuficientes para proteger al organismo de su efecto tóxico y se produce estrés oxidativo.
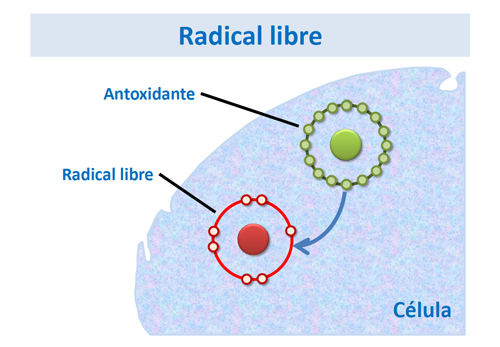
¿Qué son los radicales libres?
El cuerpo humano está formado por células y éstas a su vez por átomos y moléculas, que contienen electrones (cargas eléctricas negativas) distribuidos por pares (apareados) en su orbital externo.
Cuando un electrón no tiene pareja (está desapareado), el átomo tiene una gran tendencia a captar un electrón de otro compuesto o a perderlo para estabilizarse, es decir, se convierte en una especie muy reactiva, en un radical libre.
Este segundo compuesto al que le han “robado” un electrón se hace inestable, convirtiéndose a su vez en radical libre, y tiende a reaccionar con un tercer compuesto para estabilizarse, formándose así una reacción en cadena que puede afectar a los componentes de las membranas celulares y llegar a destruir las células, causando la muerte celular.
¿Los radicales libres tienen siempre una acción perjudicial?
No siempre, ya que también pueden actuar sobre bacterias y virus, atacando a sus membranas y defendiendo así a nuestro organismo de agentes infecciosos.
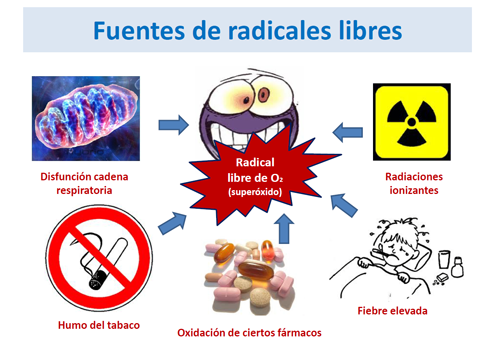
¿Cuáles son las fuentes de radicales libres?
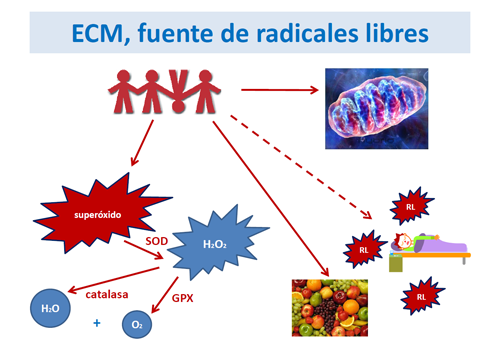
Existen unas fuentes endógenas (cuando son generados por reacciones de nuestro organismo) y unas exógenas (cuando proceden de agentes externos). Entre las endógenas la más importante es la cadena de transporte de electrónico mitocondrial (ver Enfermedades mitocondriales), cuyo funcionamiento incorrecto genera la formación de radicales libres de oxígeno.
Existen también enzimas oxidantes (xantina oxidasa) y células sanguíneas con actividad de defensa (macrófagos, etc..).
Entre los agentes exógenos destacan las radiaciones ionizantes y la luz solar, el humo del tabaco, el choque térmico, la oxidación de algunos fármacos y otras sustancias oxidoreductoras.
¿Cómo actúa nuestro cuerpo frente a la producción de un exceso de radicales libres?
Actúa contrarrestando su acción mediante mecanismos de prevención (alimentos antioxidantes), defensas antioxidantes (enzimas antioxidantes y antioxidantes no enzimáticos) y mecanismos de reparación (activación de genes que sintetizan de nuevo las proteínas dañadas por los radicales libres).
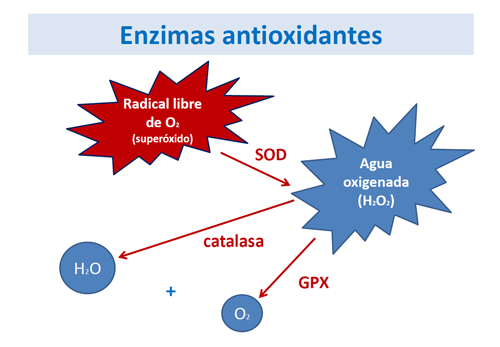
¿Qué son las enzimas antioxidantes?
Un conjunto de proteínas con función enzimática que actúan en cadena para eliminar los radicales libres.
El sistema más importante está formado por cuatro enzimas: superóxido dismutasa, glutatión peroxidasa, glutatión reductasa y catalasa, cuya función global consiste en descomponer el radical superóxido (una de las principales especies reactivas del oxígeno) en agua y oxígeno.
¿Qué son las sustancias antioxidantes?
Son sustancias capaces de ceder fácilmente electrones a los radicales libres.
Muchas de ellas son vitaminas, como la vitamina C, E y A, presentes en muchos alimentos, que tienen función antioxidante preventiva y de eliminación de radicales libres.
Otras son elementos, como el selenio (actúa de cofactor de la glutatión peroxidasa y otras enzimas), el cobre, zinc o el manganeso (cofactores de la superóxido dismutasa), y otras sustancias como el glutatión, la ubiquinona o coenzima Q10 y ciertas proteínas transportadoras de metales, como la ceruloplasmina, transferrina, ferritina y el ácido úrico.
¿Cómo puede medirse la producción de radicales libres?
Los radicales libres son difíciles de cuantificar ya que son muy reactivos e inestables, de manera que se acostumbra a valorar la variación de las actividades de las enzimas antioxidantes, la disminución de las concentraciones de las sustancias antioxidantes, la capacidad antioxidante de líquidos biológicos y tejidos, o bien el daño producido por los radicales libres sobre lípidos o proteínas mediante marcadores bioquímicos.
¿Los errores congénitos del metabolismo (ECM) son causa de estrés oxidativo?
Los ECM son enfermedades crónicas, ya que afectan al metabolismo del paciente de una forma continuada a lo largo de la vida. Muchos de ellos, los que implican al metabolismo intermediario, afectan a las reacciones de catabolismo o síntesis de pequeñas moléculas (aminoácidos, ácidos orgánicos, azúcares simples y ácidos grasos), así como a las reacciones mitocondriales de producción de energía.
En algunos de estos ECM las descompensaciones recurrentes implican una acumulación de metabolitos tóxicos, un descenso de la síntesis de biomoléculas esenciales (moléculas biológicas esenciales para la vida) y un defecto de la producción de energía.
Como la principal fuente intracelular de radicales libres es la cadena de transporte electrónico mitocondrial, su disfunción primaria (enfermedades mitocondriales) o secundaria (otros ECM que afecten su correcta función) puede generar un exceso de radicales libres.
¿Los ECM son, pues, una fuente de radicales libres?
Los ECM pueden constituir una fuente de radicales libres por diversos mecanismos: algunos metabolitos tóxicos generados son muy reactivos y actúan como radicales libres (homocisteína en la homocistinuria, fumarilacetoacetato y malelacetoacetato en la tirosinemia I), otros reaccionan con radicales libres, otros inhiben la actividad de los complejos de la cadena respiratoria (metabolitos de las acidurias propiónica y metilmalónica) o de las enzimas antioxidantes (el N-acetilaspartato inhibe la glutatión peroxidada y la catalasa en la enfermedad de Canavan, etc..), otros inhiben la síntesis de compuestos antioxidantes (metabolismo del glutatión en la cistinosis y en la tirosinemia, coenzima Q10 en la aciduria mevalónica), etc…
El algunos casos son las dietas especiales las que parecen implicadas en los bajos niveles de algunos oligoelementos (selenio en la PKU y otras enfermedades tratadas con dietas restringidas en proteínas). Son muchos los estudios realizados durante la última década para valorar el estrés oxidativo como posible mecanismo de patogenia en muchas enfermedades metabólicas.
En la tabla final se resumen algunos de los resultados de estos estudios.
Sin embargo, dado que los ECM son enfermedades minoritarias, es difícil demostrar en amplias series de pacientes unas actividades enzimáticas de las enzimas antioxidantes anormales o unas concentraciones anómalas de antioxidantes.
Muchas veces se utilizan para ello modelos animales de experimentación. Por otra parte, los resultados de estos estudios son datos indirectos, muy complejos y de difícil interpretación en muchos casos.
¿A efectos prácticos, qué acciones se pueden realizar para prevenir el estrés oxidativo en los pacientes con ECM?
En algunos ECM en los que se ha demostrado que existe una clara interferencia con la síntesis de compuestos antioxidantes, el tratamiento incluye su suplementación (vitamina E y coenzima Q10 en la aciduria mevalónica).
Pero debido a la complejidad de los mecanismos de patogenia (causantes de las manifestaciones clínicas y bioquímicas) de estas enfermedades, cualquier medida terapéutica debe estar muy bien supervisada por el médico responsable del paciente que conoce la enfermedad y sus posibilidades de tratamiento.
No obstante, como muchas sustancias antioxidantes se hallan en los alimentos (vitaminas, oligoelementos), es recomendable realizar una alimentación lo más variada posible, rica en frutas y verduras, siempre que no interfiera con el tratamiento específico del ECM (por ejemplo, en la intolerancia hereditaria a la fructosa, en que están prohibidas) y siempre aconsejados por nutricionistas responsables del paciente.
Tabla 1. Ejemplos del mecanismo de acción de algunos ECM causante de estrés oxidativo
| Defecto | Enzimas AO | SAO | Otros |
Acidurias orgánicas |
|||
| Propiónica | ↓CoQ10 | inhibe el CK y CR | |
| Metilmalónica | inhibe el CK y CR | ||
| CblC | ↑RL prevenido por B12 | ||
|
Glutárica |
↑astrocitos y disfunción mitocondrial, alteración metabolismo energético cerebral (rata) | ||
| SSADH | disfunción | alteración | |
| Ac. mevalónica | ↓GPX | ↓CoQ10 | |
| E. Canavan | ↑NAA inhibe GPX y catalasa | ↓selenio, ↓CoQ10, ↓ceruloplasmina |
↑Phe→daño DNA, ↑Phe en mPKU→↑EO en cerebro e hígado de rata |
| Alcaptonuria | ↑HGA y derivados oxidados polimerizados en tejido conectivo | ||
Aminoacidopatías |
|||
| NKH | ↓glutatión | ||
| PKU |
↓catalasa, ↓GPX |
↓selenio,↓CoQ10, ↓ceruloplasmina |
↑Phe→daño DNA, ↑Phe en mPKU→↑EO en cerebro e hígado de rata |
| Ciclo de la urea | ↑amonio→↓energía, ↑citrulina y amonio →↓capacidad oxidativa (ratón) | ||
| Tirosinemia I | ↓glutatión | Oxidación de succinilacetona | |
| HHH | ↑Orn y HCtr inhiben el CK y CR | ||
| Homocistinuria | ↑SOD | Exitotoxicidad , vulnera astrocitos, inflamación vascular y de las células gliales de la retina, mediada por SO | |
| Cistinosis | ↓glutatión | Oxidación de succinilacetona | |
| MSUD | EO en descompensaciones | ||
Defectos de los carbohidratos |
|||
| Galactosemia | ↓capacidad AO y ↑marcadores de daño DNA | ||
| Glucogenosis Ia | ↓SOD y catalasa | SO implicado en la nefropatía | |
|
Enfermedades mitocondriales |
Afectan CR | ||
| MELAS, MERRF | Mutaciones mDNA→↓CR | ||
Def. β-oxidación |
|||
| SCAD | Muerte celular exacerbada por hipertermia,↓disfunción mitocondrial | ||
| MCAD | ↑ác.cisdecenoico→EO cerebro de rata | ||
| VLCAD | ↑Grasas→↑EO | ||
E. lisosomales |
|||
| MPS III | EO en cerebro y cerebelo de ratones implicado en neurodegeneración | ||
| MPS II | ↓SAO | ||
| MPS I | disfunción | EO en cerebelo y otros órganos de ratón | |
| NPC | Forma productos de oxidación del colesterol | ||
| E. Gaucher | Disregulación de la respuesta al EO, ↑marcadores EO | ||
| Ceroide lipofuscinosis | ↑SOD | ↓glutatión | EO→activación microglias en ratón |
| E. Fabry | ↑globósido→SO | ||
E. peroxisomales |
↓catalasa | Peroxidación lipídica, disfunción mitocondrial | |
| E. Refsum | ↑fitánico→↑SO | ||
| X-ALD | ↑SOD | ↑AGCML→cambios propiedades de membrana celular, peroxidación lipídica | |
| Zellweger | ↑SOD | Disfunción de CR | |
Otros ECM |
|||
| XCT | EO | ||
CK: ciclo de Krebs; CR: cadena respiratoria mitocondrial; EO: estrés oxidativo; RL: radicales libres; SOD: superóxido dismutasa; GPX: glutatión peroxidasa; SAO: sustancias antioxidantes.
Laboratorio de Metabolopatías, Hospital Sant Joan de Déu, Barcelona.
- 18007 lecturas